Experimento de Joule
Equivalente mecánico del calor
Muchas veces habrás escuchado decir que el calor es una forma de energía, pero ¿cómo se llegó a esa conclusión? Veamos...
1) El calor puede transformarse en trabajo
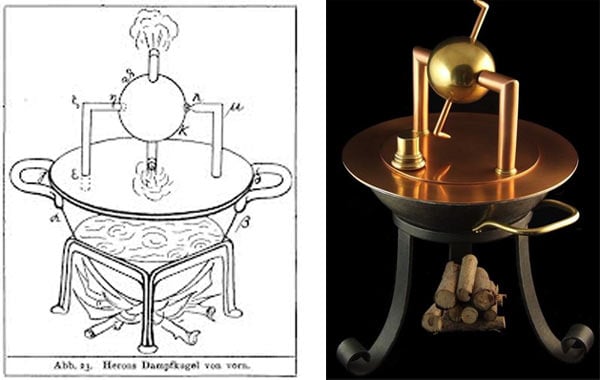
Como sabes, calentar un líquido hasta provocar su evaporación, mediante procesos de combustión, puede hacer que un plato sobre la olla baile al ritmo del vapor expulsado. Formalizar la experiencia fue la clave dar origen y perfeccionar las máquinas de vapor, mismas que modificaron considerablemente la economía y forma de vida de miles de personas durante la segunda mitad del siglo XVIII.
2) El trabajo puede convertirse en calor
Esta transformación interesó al inglés James Prescott Joule (1818-1889), quien diseñó un dispositivo que utilizó para medir cuánta energía mecánica podía transferirse a un sistema, recipiente aislado lleno de agua, a través de los cambios en su temperatura.
Dicho dispositivo consistió en un sistema pesas que, al caer, transformaban la energía potencial gravitacional, asociada a su altura, en movimiento. La energía cinética ganada era transferida al agua mediante la agitación provocada por unas aspas en el interior del calorímetro. Al analizar los cambios en la temperatura obtuvo la equivalencia de unidades conocida como equivalente mecánico del calor: 1 J = 0.24 cal.
Fuente: Maiztegui, A. y J. Sábato. (1973). La naturaleza del calor.
Introducción a la Física I. Editorial Kapelusz, Argentina. pp. 383-8.
Para entender mejor en qué consistió el experimento, puedes ver el siguiente video que muestra una reproducción, montada en pleno siglo XXI, del dispositivo utilizado por Joule en 1850.
También puedes observar una reproducción realizada con el subsidio de la Fondazione Scienza e Tecnica de Florencia, Italia.